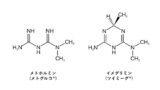
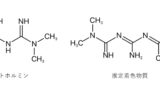
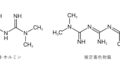
メトホルミン は非常に歴史の古い薬であるにもかかわらず、その作用機序も未だ完全に解明されていない謎の残る薬剤の一つです。
塩基性の高い化合物で、その化学的な性質が作用に重要な役割を果たしていることも近年わかってきています。
今回はビグアナイド系であるメトホルミンの化学構造とその特徴を解説します。
メトホルミンと非常に似た化学構造式で、2021年に上市されたイメグリミン(ツイミーグ®︎)と比較した記事もあるので、ぜひご参照ください。
↓↓↓
・【メトホルミンとイメグリミンの特徴と違いは?併用できる?!】化学構造式や作用機序などを比較!
メトホルミン の開発経緯と歴史
メトホルミンが日本で上市されたのは1961年と歴史が古く、今なお現場でよく使用されています。
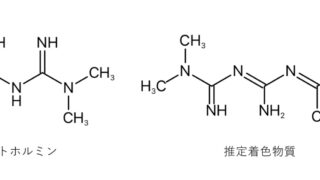
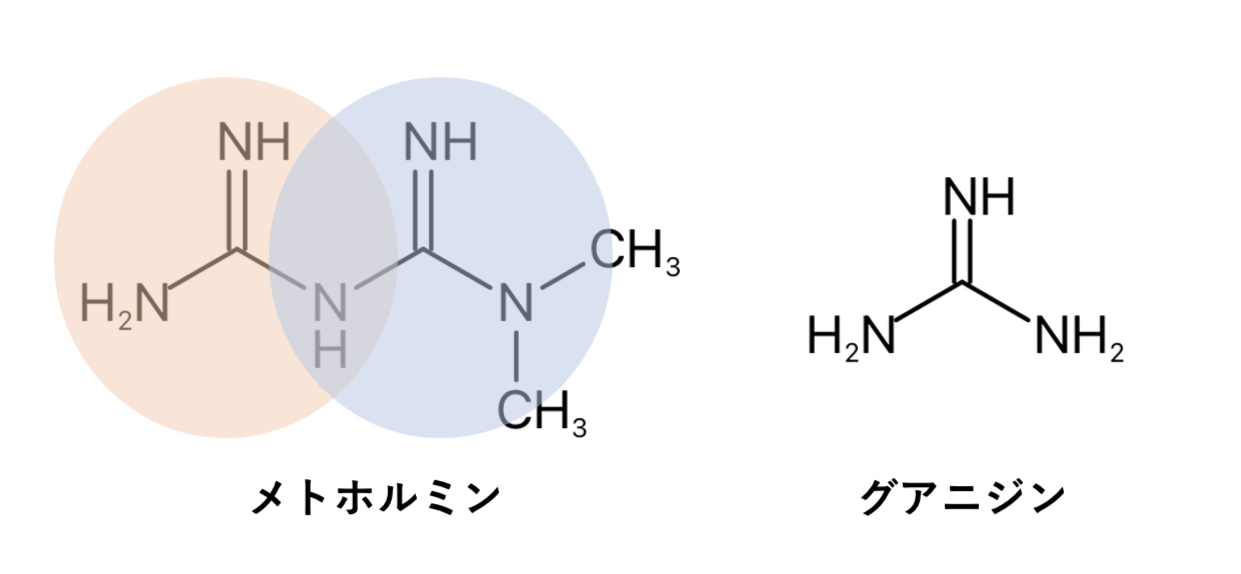
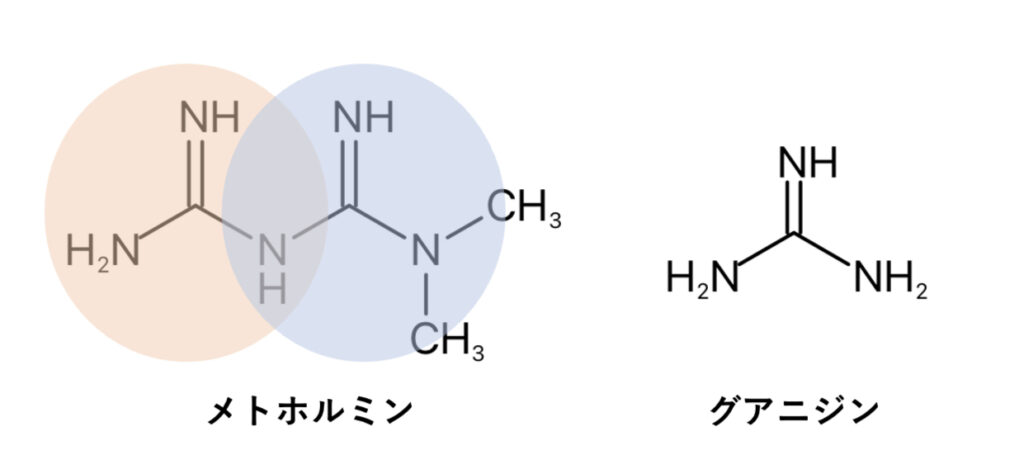
もともと植物の抽出物であるグアニジンに血糖降下作用があることから開発され、化学構造式の中に2つのグアニジン構造を持っているのが特徴です。
後に解説しますが、このグアニジンは塩基性が高く、メトホルミンが生体に作用するために重要な役割を果たしています。
メトホルミンは2014年に小児に対しての用法・用量の一部変更が認められ、2022年にはいわゆる不妊治療に対して承認を得ました。
メトホルミン の化学構造式と性質
メトホルミンの化学構造式を見るとわかるように、2つ(bi-)のグアニジン(guanidine)がくっ付いた構造で「ビグアナイド」と呼ばれるカテゴリーに属しています。
単純な構造であるにもかかわらず、未だその作用に不明な点も多く様々な研究がされています。
塩基性と水溶性
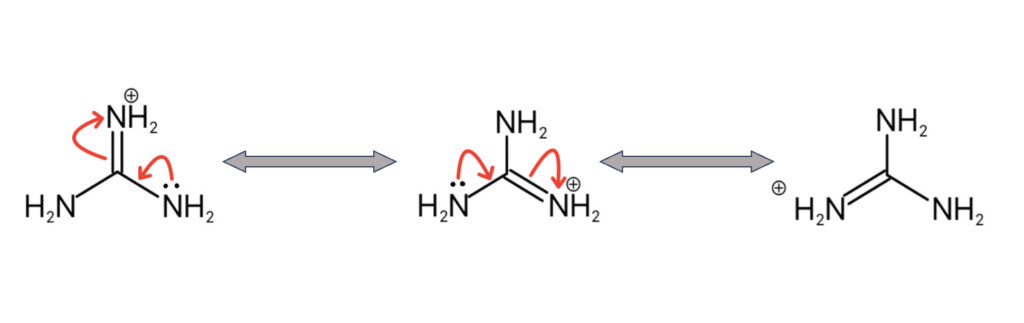
グアニジンはプロトン(H+)を捕まえると、共役酸の共鳴による安定化(電子の非局在化)でアンモニアよりも強い塩基性を示し、構造式中にアミノ基(sp3窒素)2つ、イミノ基(sp2窒素)1つを持ちます。
求核性が高い(電子を与えやすい)ことも塩基性の高さの理由です。
グアニジンは極性が高く水素結合しやすいことに加え、イオン性化合物の水溶性は上がる(脂溶性が下がる)ため、メトホルミンの水溶性が高く水に溶けやすいのも理解できます。
(※メトホルミンのインタビューフォームに分配係数の記載はありません)
メトホルミン の化学構造式と動態
次に、メトホルミンの物理化学的性質が動態にどう影響しているのか考えてみましょう!
排泄に関して、メトホルミンは分子量が小さく水溶性も高いため、ほとんど代謝を受けず未変化体で排泄される腎排泄型であるとわかるでしょう。
問題は吸収と分布過程です…
水溶性が高いのにバイオアベイラビリティ(BA、%)も高いのはなぜ?
では、本来ならメトホルミンは水溶性が高く消化管吸収されにくいはずなのに、なぜバイオアベイラビリティ(BA;生体利用率、%)が60.6%と比較的高いのでしょうか?
これは「トランスポーター」の影響と考えられています。
メトホルミンは共鳴により共役酸が安定化して強い塩基性を示し、さらに生体内で+電荷(カチオン)を持つ化合物であるため、有機カチオントランスポーター(OCT)の基質になりやすいのです。
小腸の吸収過程では、このOCTだけでなく「PMAT」と呼ばれるカチオントランスポーターも寄与することが示唆されています。
メトホルミン と 有機カチオントランスポーター(OCT)
有機カチオントランスポーター(Organic Cation Transporter; OCT)は有機カチオン化合物を輸送するトランスポーターで、+電荷をもつカチオン性の化合物を基質にします。
メトホルミンは生体内pHで+電荷(カチオン)となり、肝臓:OCT1、腎臓:OCT2がメトホルミンの輸送に寄与しています。
メトホルミンの作用は、肝細胞ミトコンドリア内のメトホルミン濃度が高いほど発揮されるため、このOCT1がメトホルミンの効果に大きく寄与しているのではないかとされています。
(メトホルミンの血糖降下作用が用量依存的に増強するとされていることとも合致します)
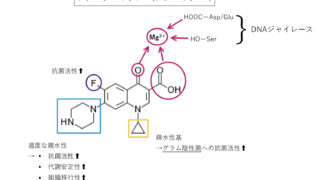
OCTがメトホルミンを基質と認識し輸送するためにはトランスポーターの芳香族アミノ酸残基とのカチオン–π相互作用が重要で、とりわけチロシン(Tyr)、トリプトファン(Trp)、フェニルアラニン(Phe)の側鎖芳香環が相互作用しやすいようです(下図)。
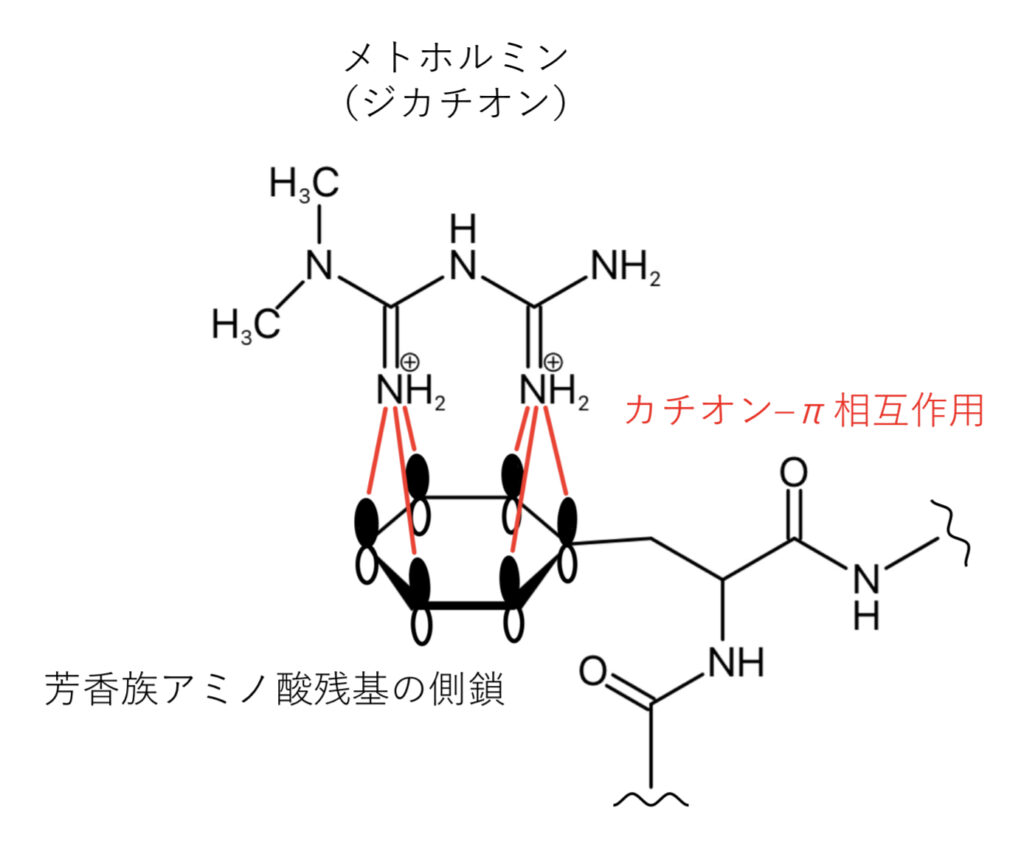
メトホルミン の作用機序
では、改めてメトホルミンの作用機序について確認してみましょう!
従来から複数の作用機序が考えられていました。
- AMPK活性化
①肝臓における糖新生の抑制
②骨格筋・脂肪組織における糖取り込み促進 - 小腸での糖吸収抑制
また、2021年にメトホルミンの化学構造に非常に似たイメグリミン(ツイミーグ®︎)が上市され、ミトコンドリア機能にかかわる作用機序が重なることもわかってきました。
イメグリミン(ツイミーグ®︎)との比較については下の記事もご参照ください。
↓↓↓
【メトホルミンとイメグリミンの特徴と違いは?併用できる?!】化学構造式や作用機序などを比較!
ミトコンドリア呼吸鎖複合体Ⅰの阻害
メトホルミンの「ミトコンドリア呼吸鎖複合体Ⅰ阻害作用」によってAMPKが活性化され、酸化的リン酸化によるATP生成を抑制し、糖新生を抑制する作用が発揮されます。
また、AMPKの活性化を経て、抗がん作用の一つであるmTORを抑制するのではないかといった研究も進んでいます。
ミトコンドリア呼吸鎖複合体Ⅰに対するメトホルミンを含むビグアナイド系薬剤の結合部位はいくつかあり、ビグアナイドが持つ+電荷(カチオン)の性質が阻害の強さや毒性に影響していると考えられているようです。
ビグアナイドの性質と阻害様式
メトホルミンなどのビグアナイドは生体内pHで2つの+電荷を持つジカチオンの状態となり、これがミトコンドリア内のビグアナイドの蓄積を促進し、呼吸鎖複合体Ⅰへの親和性が弱いながらも作用を発揮するのに十分な濃度を得ていることにつながっているようです。
阻害活性は
①膜不活性な複合体Ⅰが多いほど強い
②pHが高いほど強い
といった傾向があります。
ビグアナイドが不活性な複合体Ⅰに結合しやすいことは、周囲のアミノ酸の立体的・電気的なバランスを崩したり、活性化状態で正常にはたらく複合体Ⅰを持つミトコンドリア呼吸を崩すなどのリスクを減らすことにつながっています。
さらに、生体内ではネガティブフィードバック機構によってミトコンドリア呼吸鎖を完全に阻害してしまうリスクを減らしているとも考えられています。
個人的には、ミトコンドリア呼吸鎖を阻害しATP生成を抑制するのは機序的になかなか細胞毒な気がしていましたが、体内では見事に上手く機能していたのだと驚いています、、
追記. メトホルミン の配合変化(第105回薬剤師国家試験 問210–211)
薬剤師国家試験でもメトホルミンの化学の問題は出ていて、オルメサルタンとの一包化の問題は有名でしょう。
詳しい反応機構などはこちらの記事で解説しています!
↓↓↓
【メトホルミンとオルメサルタンの一包化で着色?!】配合変化の反応機構を解説!

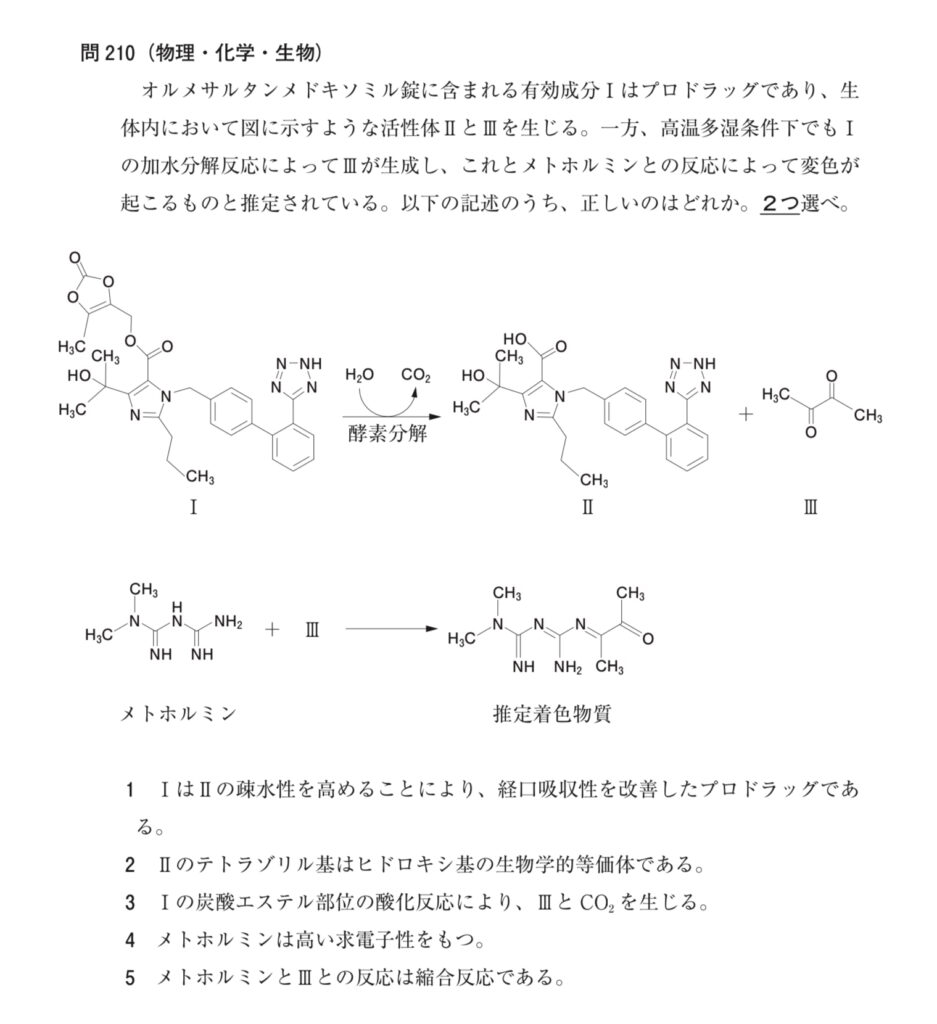

正答. 問210→1, 5、問211→4
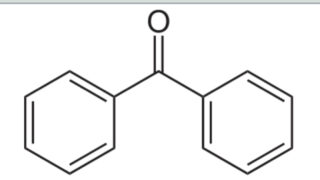
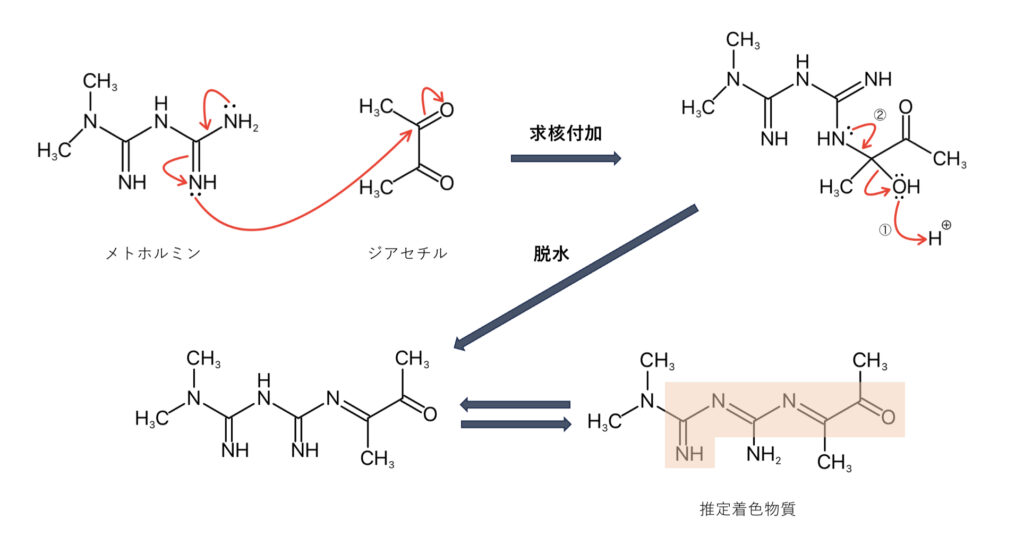
オルメサルタンのメドキソミル基が脱炭酸、加水分解を受けて生成したジアセチルがメトホルミンと脱水縮合反応を起こし、着色物質を生成するようです。
比較的長い共役二重結合が光による影響を受けやすいことも知っておくと良いでしょう!
参考:
- Mingyan Zhou, et al. Metformin transport by a newly cloned proton-stimulated organic cation transporter (plasma membrane monoamine transporter) expressed in human intestine. Drug Metab Dispos. 2007 Oct ; 35 (10) 1956-1962
- メトグルコ®︎錠インタビューフォーム
- Benoit Violet, et al. Cellular and molecular mechanisms ofmetformin: an overview. Clinical Science (Lond). 2012 Mar;122(6):253-70.
- Leydy Cano, et al. Diffusion Mechanism Modeling of Metformin in Human Organic Cationic Amino Acid Transporter one and Functional Impact of S189L, R206C, and G401S Mutation. Front Pharmacol. 2021 Feb 9:11:587590.
- Scott A Gabel, et al. A structural basis for biguanide activity. Biochemistry. 2017 Sep 12;56(36): 4786-4798.
- Hannah R Bridges, et al. Structural basis of mammalian respiratory complex I inhibition by medicinal biguanides. Science. 2023 Jan 27;379(6630):351-357.